Os ácidos podem ser classificados segundo vários critérios, vejamos:
Presença de oxigênio:
1. Hidrácidos – ácidos que não possuem oxigênio.
Exemplos: HI (ácido iodídrico), HCl (ácido clorídrico), HCN (ácido cianídrico).
2. Oxiácidos – ácidos que possuem oxigênio.
Ex: HNO3 (ácido nítrico), H2SO4 (ácido sulfúrico), H3PO4 (ácido fosfórico).
Volatilidade:
- Ácidos Voláteis – apresentam tendência à evaporação.
Exemplos: CH3COOH (ácido acético), HF (ácido fluorídrico), Hidrácidos em geral.
O vinagre (ácido acético) é um exemplo de ácido altamente volátil, quando abrimos um recipiente que o contém logo sentimos seu odor característico.
- Ácidos Fixos – apresentam pequena tendência à evaporação.
Exemplos: H2SO4 (ácido sulfúrico), H3PO4 (ácido fosfórico). Os Oxiácidos em geral não são voláteis.
Número de hidrogênios ionizáveis:
Essa classificação diz respeito à ionização de hidrogênios (H) presentes em ácidos. O número de H ionizável será a mesma quantidade de átomos de H na molécula.
• Monoácidos: possuem um único átomo de hidrogênio por molécula, portanto, apenas 1 "H" ionizável.
Exemplos: HCl (ácido clorídrico), HClO4 (ácido perclórico).
• Diácidos: possuem 2 "H" ionizáveis.
Exemplos: H2CrO4 (ácido crômico), H2CO3 (ácido carbônico).
• Triácidos: possuem 3 "H" ionizáveis.
Exemplos: H3SbO4 (ácido antimônico), H3AsO4 (ácido arsênico), H3[Fe(CN)] – ácido ferricianídrico.
• Tetrácidos: possuem 4 "H" ionizáveis.
Exemplo: H4P2O7 (ácido pirosfórico)
QUÍMICA LEGAL
Bem-vindos ao mais atualizado e inovador blog de aprendizado.Confira e aprenda de um modo dinâmico e divertido a mais temerosa QUÍMICA.
Total de visualizações de página
terça-feira, 26 de novembro de 2013
segunda-feira, 25 de novembro de 2013
Ácido acético
O ácido acético é um líquido incolor de cheiro irritante e penetrante e sabor azedo, que é quimicamente denominado de ácido etanoico e sua fórmula estrutural está demonstrada a seguir:
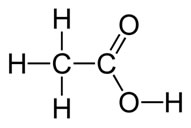


Veja que ele é um composto que pertence ao grupo orgânico dos ácidos carboxílicos.
Ele é o principal constituinte do vinagre, que é uma solução aquosa de 4 a 10% em massa de ácido acético. Ele foi obtido pela primeira vez por meio do etanol do vinho, que se oxida com o oxigênio presente no ar. Daí a origem do seu nome, pois vinho azedo vem do latim acetum que significa “vinagre”.
O uso desse composto é muito antigo, inclusive, as legiões romanas que conquistaram grande parte do mundo, conhecidas no século III a.C., marchavam longas distâncias e levavam consigo um frasco contendo vinho azedo diluído. Essa mistura de ácido acético estimulava a salivação dos soldados e diminuía a sensação de sede.

Hoje em dia, a indústria costuma usar o mesmo princípio, isto é, a oxidação do etanol (álcool etílico), para se produzir esse ácido:
H3C ─ CH2 ─ OH + O2 (ar) → H3C ─ COOH + H2O
Etanol oxigênio ácido acético ou etanoico água
Etanol oxigênio ácido acético ou etanoico água
No caso do vinagre, essa oxidação mostrada na reação química acima é obtida por meio de fermentação, com o auxílio do fungo Mycoderma aceti (chamado mãe do vinagre) e da enzima alcooloxidase. Podem-se usar também bactérias do gênero Acetobacter e Clostridium acetobtylicum. Porém, outro meio é o uso de um catalisador como o pentóxido de divanádio (V2O5).
Pode-se também produzir o ácido acético por meio da oxidação do metanol, pela destilação da madeira e a partir de derivados do petróleo.
Além de ser usado como tempero na alimentação, o acido acético também é usado na produção de acetato de vinila (para se fazer o polímero PVA), de anidrido acético e cloreto de acetila (usados em sínteses orgânicas), de ésteres (solventes, perfumes, essências, entre outros), de acetato de celulose (fibras têxteis), de acetatos inorgânicos etc.
Quando está na sua forma pura é chamado de ácido acético glacial, pois se solidifica a temperatura de 16,7ºC, ficando com o aspecto de gelo.
sexta-feira, 22 de novembro de 2013
A vitamina do banho de sol!!!!
O sol é taxado como um vilão para a saúde e de fato é perigoso, quando tem ação prolongada sobre a pele pode levar ao temido câncer de pele. O que não se pode confundir é um Banho de sol de qualidade com uma insolação.
O que mais se ouve por aí é que para manter a saúde corporal é preciso manter uma dieta balanceada, fazer muito exercício físico, ingerir somente alimentos saudáveis, todos estes requisitos fazem parte do processo, mas não são suficientes para se alcançar a vitalidade. Pelo contrário, o que estamos sugerindo neste contexto não diz respeito a sacrifício algum, como passar fome, resistir a doces, ficar exausto de malhar, bastariam apenas 15 minutos diários de uma prazerosa tarefa: vestir uma roupa de banho e curtir o sol a beira de uma piscina!
Mas o que tem de tão especial nesta ação? Trata-se da vitamina presente nos raios solares que está envolvida em diversas funções corporais, como a atividade imunológica, fortalecimento de ossos, desenvolvimento embrionário, inibidor de câncer, entre outras. Estamos falando da vitamina D, ela se faz presente também em alimentos como o salmão, por exemplo, nesta forma fica difícil seu consumo, já que ninguém come este peixe todo dia. Mas no caso do sol, a vitamina é gratuita e está disponível diariamente para quem quiser.
A seguir, como é ativada a vitamina D no organismo:
As partículas de colesterol presentes nos alimentos que ingerimos são usadas para fabricar o composto 7- dehidrocolesterol, uma vez presente em nosso organismo este composto se desloca para a camada externa de nossa pele (a epiderme). Ao recebermos a radiação solar, mais precisamente os raios ultravioletas do tipo B (UVB) que penetram na pele, a molécula de 7- dehidrocolesterol passa por várias transformações químicas e dá origem à vitamina D.
Para o tempo não ser uma desculpa para se isentar da vitamina D, procure realizar tarefas diárias, como ler o Jornal sentado ao sol. A roupa de banho é ideal, porque o recomendável seria deixar cerca de 30 % do corpo exposto, só não se esqueça do protetor solar.
Não dificulte a sua longevidade, divirta-se no verão: tome aquele sol vitaminado! Invista em sua saúde além de manter aquele maravilhoso bronzeado dourado.
O que mais se ouve por aí é que para manter a saúde corporal é preciso manter uma dieta balanceada, fazer muito exercício físico, ingerir somente alimentos saudáveis, todos estes requisitos fazem parte do processo, mas não são suficientes para se alcançar a vitalidade. Pelo contrário, o que estamos sugerindo neste contexto não diz respeito a sacrifício algum, como passar fome, resistir a doces, ficar exausto de malhar, bastariam apenas 15 minutos diários de uma prazerosa tarefa: vestir uma roupa de banho e curtir o sol a beira de uma piscina!
Mas o que tem de tão especial nesta ação? Trata-se da vitamina presente nos raios solares que está envolvida em diversas funções corporais, como a atividade imunológica, fortalecimento de ossos, desenvolvimento embrionário, inibidor de câncer, entre outras. Estamos falando da vitamina D, ela se faz presente também em alimentos como o salmão, por exemplo, nesta forma fica difícil seu consumo, já que ninguém come este peixe todo dia. Mas no caso do sol, a vitamina é gratuita e está disponível diariamente para quem quiser.
A seguir, como é ativada a vitamina D no organismo:
As partículas de colesterol presentes nos alimentos que ingerimos são usadas para fabricar o composto 7- dehidrocolesterol, uma vez presente em nosso organismo este composto se desloca para a camada externa de nossa pele (a epiderme). Ao recebermos a radiação solar, mais precisamente os raios ultravioletas do tipo B (UVB) que penetram na pele, a molécula de 7- dehidrocolesterol passa por várias transformações químicas e dá origem à vitamina D.
Para o tempo não ser uma desculpa para se isentar da vitamina D, procure realizar tarefas diárias, como ler o Jornal sentado ao sol. A roupa de banho é ideal, porque o recomendável seria deixar cerca de 30 % do corpo exposto, só não se esqueça do protetor solar.
Não dificulte a sua longevidade, divirta-se no verão: tome aquele sol vitaminado! Invista em sua saúde além de manter aquele maravilhoso bronzeado dourado.
quinta-feira, 21 de novembro de 2013
A química do amor!!!
Você já ouviu esta frase: Rolou uma química entre nós! Será que existe mesmo uma explicação científica para o amor?
O sentimento não afeta só o nosso ego de forma figurada, mas está presente de forma mais concreta, produz reações visíveis em nosso corpo inteiro. Se não fosse assim como explicar as mãos suando, coração acelerado, respiração pesada, olhar perdido (tipo "peixe morto"), o ficar rubro quando se está perto do ser amado?
Afinal, o amor tem algo a ver com a Química? Na verdade O AMOR É QUÍMICA! Todos os sintomas relatados acima têm uma explicação científica: são causados por um fluxo de substâncias químicas fabricadas no corpo da pessoa apaixonada. Entre essas substâncias estão: adrenalina, noradrenalina, feniletilamina, dopamina, oxitocina, a serotonina e as endorfinas. Viu como são necessários vários hormônios para sentir aquela sensação maravilhosa quando se está amando?
A dopamina produz a sensação de felicidade, a adrenalina causa a aceleração do coração e a excitação. A noradrenalina é o hormônio responsável pelo desejo sexual entre um casal, nesse estágio é que se diz que existe uma verdadeira química, pois os corpos se misturam como elementos em uma reação química.
Mas acontece que essa sensação pode não durar muito tempo, neste ponto os casais têm a impressão que o amor esfriou. Com o passar do tempo o organismo vai se acostumando e adquirindo resistência, passa a necessitar de doses cada vez maiores de substâncias químicas para provocar as mesmas sensações do início. É aí que entra os hormônios ocitocina e vasopressina, são eles os responsáveis pela atração que evolui para uma relação calma, duradoura e segura, afinal, o amor é eterno!
O sentimento não afeta só o nosso ego de forma figurada, mas está presente de forma mais concreta, produz reações visíveis em nosso corpo inteiro. Se não fosse assim como explicar as mãos suando, coração acelerado, respiração pesada, olhar perdido (tipo "peixe morto"), o ficar rubro quando se está perto do ser amado?
Afinal, o amor tem algo a ver com a Química? Na verdade O AMOR É QUÍMICA! Todos os sintomas relatados acima têm uma explicação científica: são causados por um fluxo de substâncias químicas fabricadas no corpo da pessoa apaixonada. Entre essas substâncias estão: adrenalina, noradrenalina, feniletilamina, dopamina, oxitocina, a serotonina e as endorfinas. Viu como são necessários vários hormônios para sentir aquela sensação maravilhosa quando se está amando?
A dopamina produz a sensação de felicidade, a adrenalina causa a aceleração do coração e a excitação. A noradrenalina é o hormônio responsável pelo desejo sexual entre um casal, nesse estágio é que se diz que existe uma verdadeira química, pois os corpos se misturam como elementos em uma reação química.
Mas acontece que essa sensação pode não durar muito tempo, neste ponto os casais têm a impressão que o amor esfriou. Com o passar do tempo o organismo vai se acostumando e adquirindo resistência, passa a necessitar de doses cada vez maiores de substâncias químicas para provocar as mesmas sensações do início. É aí que entra os hormônios ocitocina e vasopressina, são eles os responsáveis pela atração que evolui para uma relação calma, duradoura e segura, afinal, o amor é eterno!
quarta-feira, 20 de novembro de 2013
A poluição prejudica o desempenho dos atletas?
Esta questão foi levantada justamente por que os Jogos Olímpicos de 2008 terão como sede uma das capitais mais poluídas do mundo. Para se ter uma ideia, a cidade de São Paulo é a 3ª cidade mais poluída da América Latina, mas os atletas conseguem praticar seus esportes tranquilamente. O grande problema é que em Pequim a poluição é três vezes maior do que na capital Paulista. Os chineses estão investindo muito para contornar a situação, já foram gastos mais de 17 bilhões de dólares, e mesmo assim o Comitê Olímpico Internacional já admitiu que não se pode esperar novos recordes ao ar livre, devido à contaminação atmosférica.
A poluição com certeza vai afetar o desempenho dos atletas, é só fazer a seguinte análise: um atleta respira cerca de 20 vezes mais ar que uma pessoa comum, e na cidade de Pequim significa inspirar 4 vezes mais CO (monóxido de carbono), CO2 (dióxido de carbono e ozônio do que o corpo tolera.
O ar poluído pode gerar de cãibras a infarto, veja abaixo as consequências da poluição no organismo humano:
- O dióxido de carbono quando chega à alta concentração aos pulmões, atrapalha o trabalho das hemácias. As hemácias são as células responsáveis por levar oxigênio ao organismo.
- O monóxido de carbono rouba o lugar do oxigênio nas hemácias, os músculos podem então sofrer cãibras por falta de força. A ausência de oxigênio no cérebro causa tonturas e pode levar até mesmo ao coma.
- O ozônio prejudica a corrente sanguínea, ele possui a propriedade de converter colesterol em placas de gordura, estas grudam nos vasos sanguíneos e diminuem a flexibilidade dos mesmos. O coração passa a trabalhar sob alta pressão para continuar bombeando sangue, e isto pode causar hemorragias e infarto.
A poluição com certeza vai afetar o desempenho dos atletas, é só fazer a seguinte análise: um atleta respira cerca de 20 vezes mais ar que uma pessoa comum, e na cidade de Pequim significa inspirar 4 vezes mais CO (monóxido de carbono), CO2 (dióxido de carbono e ozônio do que o corpo tolera.
O ar poluído pode gerar de cãibras a infarto, veja abaixo as consequências da poluição no organismo humano:
- O dióxido de carbono quando chega à alta concentração aos pulmões, atrapalha o trabalho das hemácias. As hemácias são as células responsáveis por levar oxigênio ao organismo.
- O monóxido de carbono rouba o lugar do oxigênio nas hemácias, os músculos podem então sofrer cãibras por falta de força. A ausência de oxigênio no cérebro causa tonturas e pode levar até mesmo ao coma.
- O ozônio prejudica a corrente sanguínea, ele possui a propriedade de converter colesterol em placas de gordura, estas grudam nos vasos sanguíneos e diminuem a flexibilidade dos mesmos. O coração passa a trabalhar sob alta pressão para continuar bombeando sangue, e isto pode causar hemorragias e infarto.
terça-feira, 19 de novembro de 2013
Momento de rir!!!!
P: 2 ursos são jogados na água mas só um dissolve, porque?
R: Porque ele era um urso polar!
P: O que seis carbonos estão fazendo de mãos dadas com seis hidrogênios na igreja?
R: Benzeno!
P: Porque o martelo e a tesoura são hidrocarbonetos?
R: Porque o martelo é propino e a tesoura é propano!
R: Porque ele era um urso polar!
P: O que seis carbonos estão fazendo de mãos dadas com seis hidrogênios na igreja?
R: Benzeno!
P: Porque o martelo e a tesoura são hidrocarbonetos?
R: Porque o martelo é propino e a tesoura é propano!
segunda-feira, 18 de novembro de 2013
Assinar:
Postagens (Atom)